Claire Lafourcade a,b,c, Olivia Kérourédan a,b,c
a Université de Bordeaux, UFR des Sciences Odontologiques de Bordeaux, Bordeaux, France
b CHU de Bordeaux, Pôle de Médecine et Chirurgie bucco-dentaire, Bordeaux, France
c Université de Bordeaux, INSERM, BioTis, U1026, Bordeaux, France
Un problème quotidien… et croissant
L’hyperesthésie dentinaire est un motif de consultation de plus en plus fréquent. Cette douleur brève mais intense, déclenchée par un simple contact ou un verre d’eau froide, impacte significativement la qualité de vie des patients [1]. D’étiologie plurifactorielle, elle est le plus souvent liée à un brossage traumatique ou à des processus d’érosion dentaire. Son diagnostic peut s’avérer complexe, exigeant rigueur et méthode dans la prise en charge (fig. 1).
 Figure 1
Figure 1De quoi s’agit-il ?
L’hyperesthésie dentinaire (HD), plus souvent connue sous le terme d’hypersensibilité dentaire, est définie comme une « douleur brève, vive et aiguë ressentie au niveau de la dentine exposée en réponse à des stimuli thermiques, évaporatifs, tactiles, osmotiques ou chimiques et ne pouvant pas être attribuée à toute autre forme d’anomalie ou de pathologie dentaire » [2].
Trois théories ont été évoquées pour expliquer cette douleur [3]:
- Théorie nociceptive : activation directe des terminaisons nerveuses présentes dans la dentine.
- Théorie hydrodynamique de Brännström : déplacement du fluide dentinaire à l’intérieur des tubules stimulant les terminaisons nerveuses (fig. 2).
La théorie hydrodynamique de Brannstrom
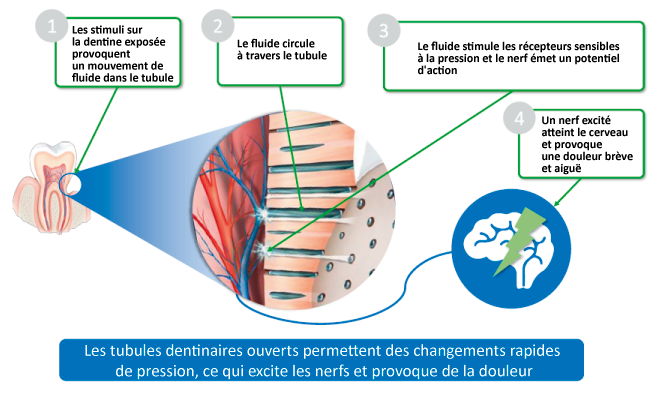
- Théorie odontoblastique : les odontoblastes seraient des cellules sensorielles capables de moduler la transduction de la douleur dans les fibres nerveuses de la pulpe dentaire.
Aujourd’hui, on considère que les mécanismes de l’HD impliqueraient un couplage des théories hydrodynamique et odontoblastique [3].
Comment la diagnostiquer ?
Le diagnostic de l’HD repose sur un interrogatoire et un examen clinique rigoureux afin d’orienter vers une prise en charge optimale permettant la disparition des symptômes [4]. Il est basé sur un diagnostic d’exclusion visant à éliminer l’ensemble des autres causes pouvant être à l’origine d’une douleur pulpaire [2].
Lors de l’interrogatoire, les éléments suivants sont à recueillir [3] :
- Habitudes alimentaires (prise d’aliments ou boissons acides, énergétiques) ;
- Habitudes d’hygiène buccodentaire HBD (fréquence et technique de brossage, type de brosse à dents utilisée) ;
- Antécédents médicaux et médications acides ou sialoprives (psychotropes, anticholinergiques) ;
- Pathologies (troubles du comportement alimentaire (TCA), reflux gastro-œsophagiens (RGO)) ;
- Environnement professionnel et pratiques sportives (industrie chimique, œnologie, respiration buccale, piscine chlorée) ;
- Xérostomie, parafonctions, habitudes nocives (tabac, alcool).
Il est important de caractériser la douleur et d’évaluer son intensité avec des échelles adaptées pour pouvoir évaluer l’efficacité des traitements qui seront mis en place [2].
Un examen clinique doit être fait avec des aides optiques afin de relever les éléments suivants : indice carieux, indice de plaque, biotype parodontal, présence d’inflammation gingivale, récessions et/ou érosions généralisées. L’examen est ensuite orienté vers la zone douloureuse afin de détecter une surface dentinaire exposée suite à une récession associée à une perte d’émail et/ou de cément [3].
Les examens complémentaires à la disposition du praticien sont les suivants :
- Reproduction de la douleur via un stimulus tactile, thermique ou évaporatif ;
- Utilisation d’indices tels que l’indice de Schiff quantifiable en utilisant le test évaporatif sur une échelle de 0 à 3 selon la gravité (0 : pas de réponse, 1 : réponse au stimulus mais pas de demande d’arrêt de celui-ci, 2 : réponse au stimulus et demande de son arrêt ou évitement, 3 : réponse douloureuse au stimulus et demande d’arrêt) [3].
Quelles étiologies et facteurs de risque ?
La récession gingivale et l’exposition dentinaire sont les deux facteurs étiologiques principaux à l’origine d’une communication entre le tissu pulpaire et l’environnement oral [3].
- Récession gingivale liée à des facteurs prédisposants (phénotype fin, malposition), déclenchants (plaque, maladie parodontale, habitude nocive, LCNC*), aggravants (traumatisme occlusal, orthodontie) ou physiologiques (âge).
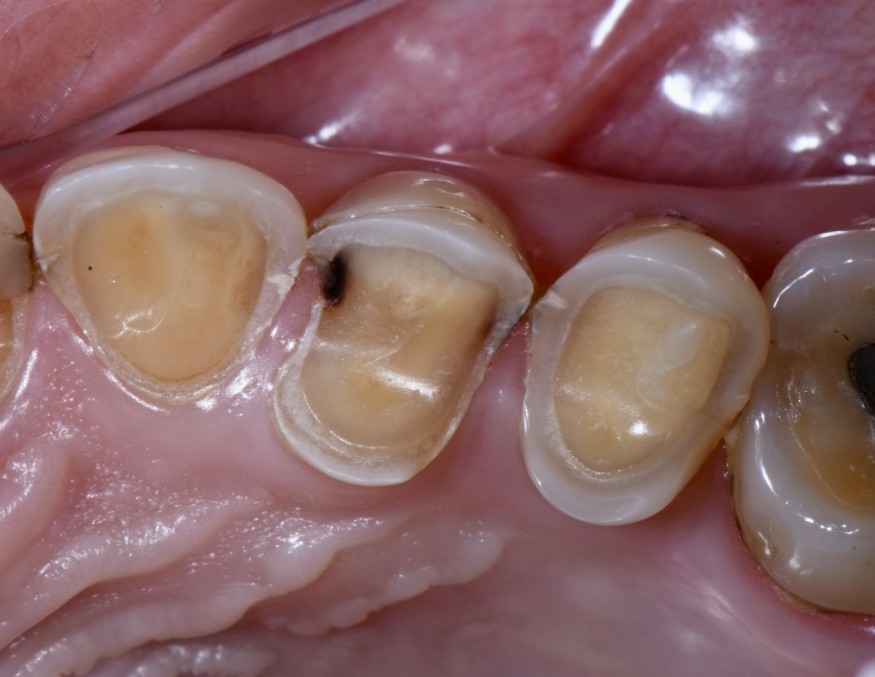
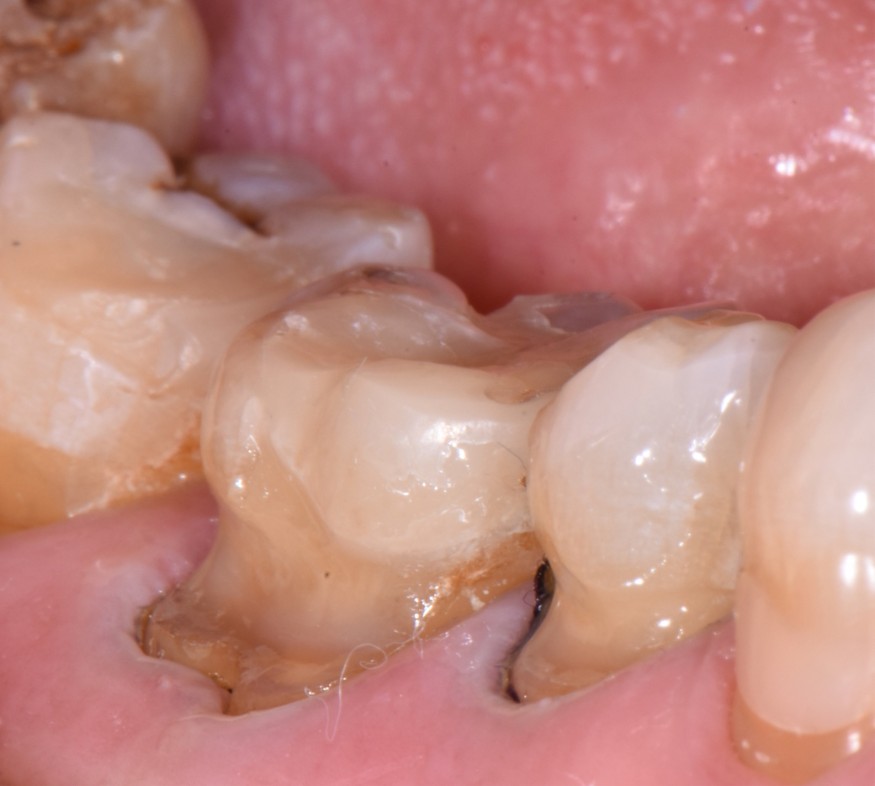
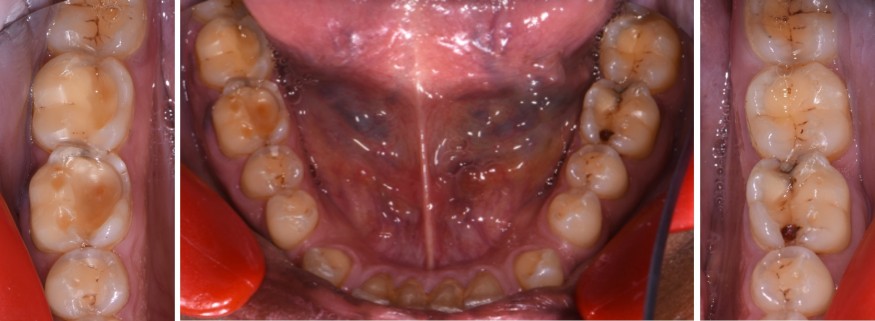
- Exposition dentinaire, due à la perte d’émail ou de cément, par abrasion (brossage traumatique), érosion (acides), attrition (bruxisme) (fig. 3-7), ou anomalies de structure (MIH**, amélogenèse imparfaite) [5].
L’HD peut aussi être induite par des soins dentaires tels que l’éclaircissement, les thérapeutiques parodontales ou encore les préparations prothétiques sur dents vitales.
Comment la prendre en charge ?
La stratégie s’appuie sur le concept de gradient thérapeutique : éducation thérapeutique et traitements non invasifs en ambulatoire, puis application de topiques, et en dernier recours soins invasifs [4,6-8].
Les options disponibles sont basées sur 2 principes : désensibilisation des terminaisons nerveuses à l’aide d’ions potassium et obturation des tubuli dentinaires (blocage du mécanisme hydrodynamique).
- Première intention :
- Éducation thérapeutique avec conseils d’HBD, révision des méthodes de brossage, conseils diététiques, orientation vers spécialiste (si présence de RGO ou de TCA…).
- Prescription d’agents désensibilisants pendant 3 à 4 semaines (puis au long cours) en insistant sur la nécessité d’observance de la part du patient (dentifrices ou solutions à base de fluorures stanneux, fluorures d’amine, arginine et carbonate de calcium, acétate de strontium et fluorure de sodium et calcium phosphosilicate (NovaMin), nitrate de potassium ainsi que des gels et mousses à base de fluorure stanneux, CPP-ACP (caséine phosphopeptide – amorphous calcium phosphate).
- Seconde intention :
- Applications professionnelles au fauteuil : vernis fluorés, agents adhésifs désensibilisants (polymères additionnés de calcium et oxalates, glutaraldéhyde et méthacrylate de hydroxyéthyle) ou laser (fermeture des tubuli par coagulation des protéines du fluide tubulaire).
- Dernière intention :
- Traitements invasifs non spécifiques de l’HD : restaurations en résine composite, chirurgie mucogingivale, traitement endodontique en dernier recours.
Un suivi à court, moyen et long terme est essentiel pour contrôler les facteurs de risque, réévaluer l’efficacité des traitements et ajuster la prise en charge [3].
À retenir :
-
- L’HD est un diagnostic par exclusion.
- Deux causes principales : récession gingivale et exposition dentinaire.
- La prise en charge est progressive : prévention ➜ désensibilisation ➜ traitements ciblés.
- Le traitement étiologique reste la clé d’un résultat durable.
* lésions cervicales non carieuses
** hypominéralisation des molaires et des incisives
Bibliographie
- Douglas-de-Oliveira DW, Vitor GP, Silveira JO, Martins CC, Costa FO, Cota LOM. Effect of dentin hypersensitivity treatment on oral health related quality of life — A systematic review and meta-analysis. Journal of Dentistry. avr 2018;71:1‑8.
- Kérourédan O, Ziane S, Devillard R. Pourquoi et comment traiter l’hyperesthésie dentinaire. Actualités Pharmaceutiques. nov 2020;59(600):52‑6.
- Devun M, Bret F, Ziane-Casenave S, Devillard R, Doméjean S, Maurin JC, et al. Hyperesthésie dentinaire : concepts et stratégies thérapeutiques. EMC [Internet].juin 2022 [cité 10 mars 2025];15(3). Disponible sur: http://www.crossref.org/deleted_DOI.html
- Devillard R, Romieu O, Arbab-Chirani R, Colon P, Mortier É, Seux D. Hypersensibilité dentinaire. Référentiel de l’internat – Dentisterie restauratrice et endodontie. Paris : L’information dentaire.2021;84‑90.
- Massé L, Lesieur C, Collignon AM, Kérourédan O. CONNAÎTRE – L’usure dentaire érosive : mieux la comprendre pour mieux la diagnostiquer.CLINIC. nov 2023;431.
- Clark D, Levin L. Non-surgical management of tooth hypersensitivity. International Dental Journal. oct 2016;66(5):249‑56.
- Liu XX, Tenenbaum HC, Wilder RS, Quock R, Hewlett ER, Ren YF. Pathogenesis, diagnosis and management of dentin hypersensitivity: an evidence-based overview for dental practitioners. BMC Oral Health. déc 2020;20(1):220.
- West NX, Seong J, Davies M. Management of dentine hypersensitivity: efficacy of professionally and self‐administered agents.J Clinic Periodontology [Internet]. avr 2015 [cité 11 avr 2025];42(S16). Disponible sur: https://onlinelibrary.wiley.com/doi/10.1111/jcpe.12336
Légendes
- Figure 1. Illustration de l’impact de l’hyperesthésie dentinaire sur la vie quotidienne.
(Source : HALEON Group) - Figure 2. Schéma illustrant la théorie hydrodynamique de Brännström.
(Source : HALEON Group) - Figure 3. Lésions érosives sévères associées à des lésions carieuses chez une patiente souffrant d’une addiction aux sodas.
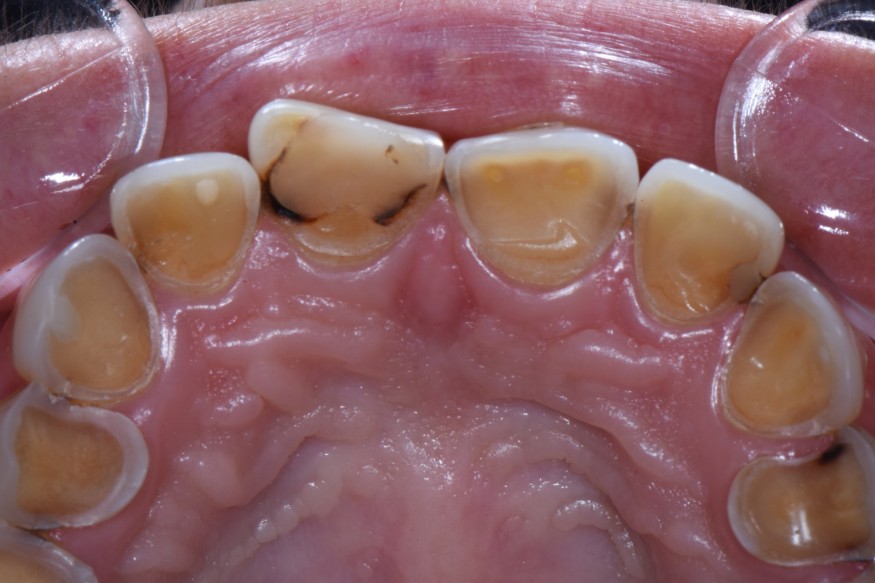
(Crédit photo : Olivia Kérourédan) - Figure 4. Lésions érosives palatines au niveau du secteur incisivo-canin maxillaire, suggérant une acidité d’origine endogène.
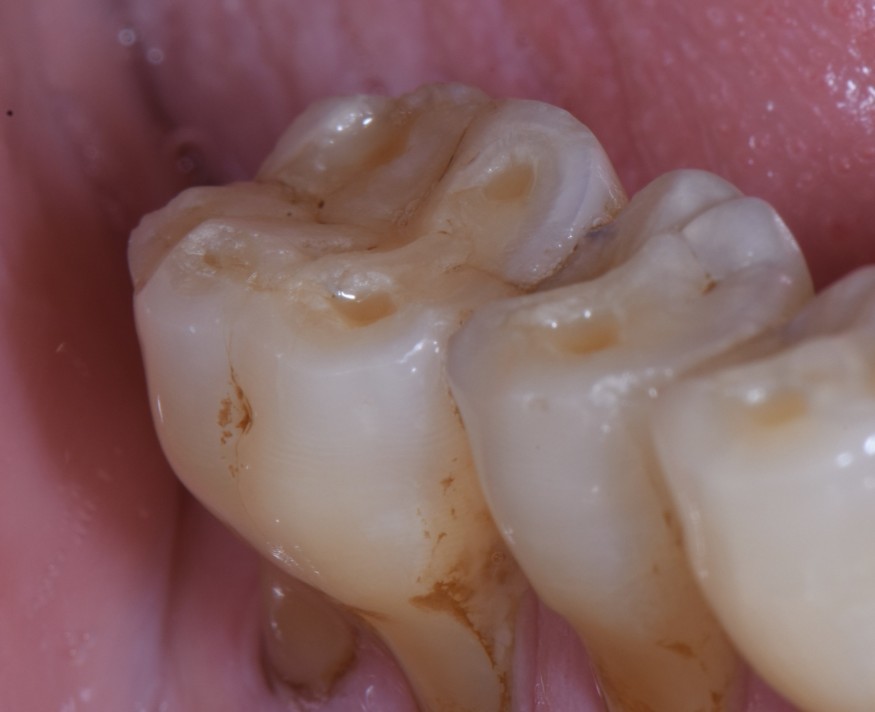
(Crédit photo : Olivia Kérourédan) - Figure 5. Association de lésions d’usure d’origine érosive, abrasive et attritionnelle.
(Crédit photo : Olivia Kérourédan) - Figure 6. Lésions d’usure typiques provoquées par des phénomènes d’abrasion.
(Crédit photo : Olivia Kérourédan) - Figure 7. Asymétrie des lésions érosives constatée chez une patiente souffrant de reflux gastro-œsophagiens.
(Crédit photo : Olivia Kérourédan)










Commentaires