Pr Marjolaine GOSSET PU-PH, Université Paris Cité, Service de Médecine bucco-dentaire, Hôpital Rothschild AP-HP, UMRS 1333 Inserm Université Paris Cité.
En 2017, la Fédération Européenne de Parodontologie (EFP) et l’Association Américaine de Parodontologie (AAP) ont adopté à Chicago la nouvelle classification mondiale des maladies et affections parodontales et péri-implantaires [1]. Les données de la littérature ainsi que l’utilisation clinique montraient les limites de la précédente classification dite d’Armitage, adoptée en 1999 [2]. Citons, pour exemple, l’absence de preuves d’une physiopathologie spécifique qui permet de différencier cliniquement les cas de parodontite « agressive » ou « chronique » et de les traiter différemment, ou encore une classification qui ne tenait pas compte des caractéristiques cliniques spécifiques de la maladie chez le patient, et qui influencent le traitement (ex. : profondeur de poches, présence de lésions inter-radiculaires).
Depuis l’adoption de cette nouvelle classification, l’EFP a mené un travail conséquent lors de workshops internationaux pour définir, dans une démarche de dentisterie basée sur les preuves scientifiques (« evidenced based dentistry »), des recommandations pour le traitement des parodontites [3, 4]. Ces recommandations ont notamment été reconnues pour la France par la Société Française de Parodontologie et Implantologie Orale (SFPIO) et par le Collège National des Enseignants en Parodontologie (CNEP).
Dans cet article, nous allons centrer nos propos sur la définition des états de santé et de maladies parodontales (gingivite, parodontite) en accord avec la classification de Chicago parue en 2017, tout en présentant la structuration des étapes pour le traitement des parodontites de stade I à III, telles que recommandées par l’EFP.
Les points principaux de la classification de Chicago, 2017
SANTÉ PARODONTALE, GINGIVITE ET PARODONTITE
La classification de Chicago se caractérise en premier lieu par la définition d’un état de santé parodontale, de la gingivite et de la parodontite [5]. Il est important de noter que le patient atteint de parodontite, qu’on peut nommer patient parodontal, pourra recouvrer une santé parodontale, mais restera à risque de récidive toute sa vie (fig. 1). La maintenance parodontale visera à prévenir cette récidive de la maladie.
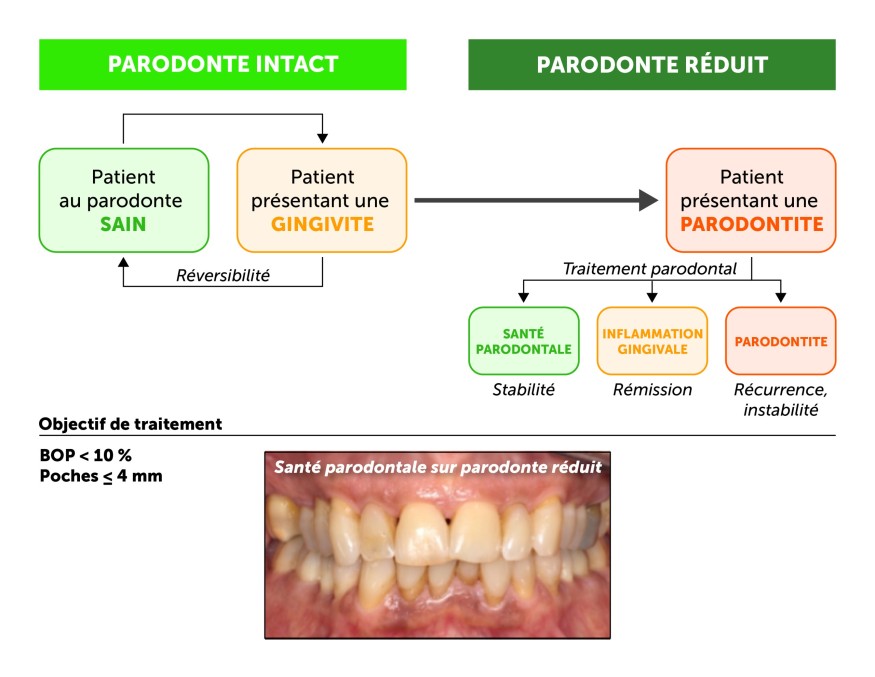
Figure 1. Relation entre les états de santé parodontale chez le patient parodontal(adapté de Chapple I et al, J Periodontol, 2018)
§BOP : Bleeding On Probing : saignement au sondage
Les définitions suivantes sont proposées (fig. 2) :
> la santé parodontale se définit cliniquement par l’absence de signes d’inflammation gingivale ou d’autres symptômes décrits par le patient (halitose, saignements gingivaux…). L’utilisation d’indices parodontaux (relevés en 6 points par dent lors du bilan parodontal) permet de caractériser cette santé parodontale : il s’agit du saignement au sondage < 10 % et d’une profondeur de sondage ≤ 3 mm. Cependant, pour le patient parodontal, il sera accepté des profondeurs de poches allant jusqu’à 4 mm. Ces critères seront donc à retrouver à l’issue du traitement parodontal pour pouvoir dire que le patient parodontal est stabilisé (tab. 1) ;
> la gingivite se définit, par opposition à la santé parodontale, par l’observation de signes cliniques d’inflammation associés à d’éventuels signes rapportés par le patient et la présence de saignements au sondage ≥ 10% sans poche parodontale (tab. 1). L’état de gingivite peut exister chez le patient sans antécédent de parodontite, le patient présentant un parodonte réduit suite à des interventions de type élongation coronaire, ou chez le patient parodontal.
Tableau 1. Les états de santé parodontale et gingivite chez le patient non parodontal et le patient parodontal.
* Force de sondage : 20 à 25 grammes ; pas de pseudo-poches ; ** Un parodonte réduit sans antécédent de parodontite correspond à un parodonte suite à une élongation coronaire par exemple.
> la parodontite fait l’objet de la section suivante. Notons que trois formes différentes ont été identifiées [1] : 1- la parodontite nécrosante, 2- la parodontite comme une manifestation directe d’une maladie systémique (ex. : cas d’une parodontite associée à une hypophosphatémie qui altère le cément et donc le système d’attache) et 3- la parodontite, regroupant les formes précédemment décrites comme « chroniques » et « agressives ». Un système multidimensionnel de stades et de grades a été mis au point pour mieux décrire les formes cliniques de la parodontite [6] : les stades (I à IV) reposent sur la gravité et l’étendue de la maladie ; les grades (A à C) décrivent le taux de progression probable.
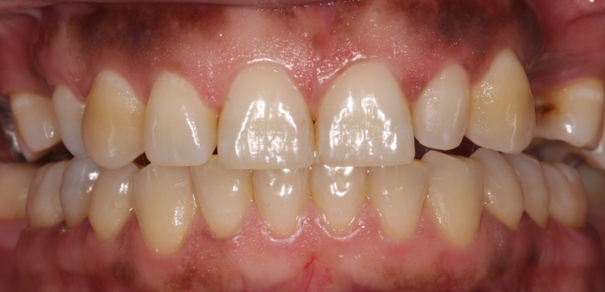
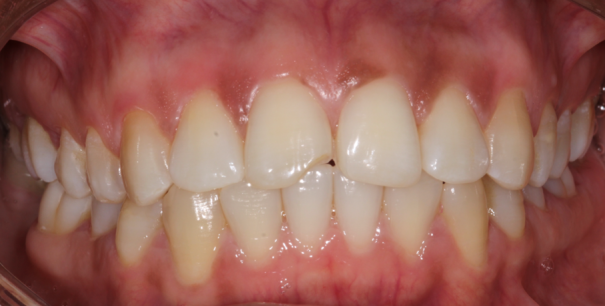
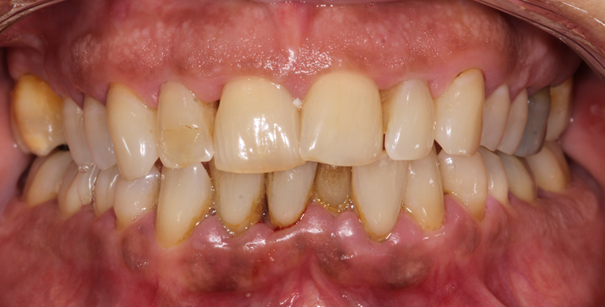
Figure 2. Cas cliniques de santé parodontale (A), gingivite (B), parodontite (C). (A) Patiente âgée de 45 ans, en bonne santé générale et non fumeuse, présentant une santé parodontale, sans antécédent de parodontite ou de parodonte réduit. On observe ici les caractéristiques de la santé gingivale (festonnée, ferme, piqueté, rose pâle). La patiente ne rapporte aucun saignement. L’examen parodontal ne décèle aucune poche, aucune perte d’attache et un BOP = 6 %. (B) Patiente âgée de 21 ans, en bonne santé générale, non fumeuse, enceinte, présentant une gingivite, sans antécédent de parodontite ou de parodonte réduit. On observe ici une inflammation papillaire tandis que l’examen parodontal ne décèle aucune poche, aucune perte d’attache mais un BOP = 32 % (la patiente présente également une épulis palatine au niveau de 24/25). (C) Patiente âgée de 48 ans, en bonne santé générale, fumeuse (10 cigarettes/jour depuis 20 ans), présentant une parodontite. On observe ici une inflammation gingivale sévère mandibulaire, plus discrète au maxillaire, ainsi qu’une perte de papilles interdentaires. La patiente rapporte des saignements au brossage et une halitose. Un examen parodontal révèle des poches parodontales généralisées allant jusqu’à 8 mm et des pertes d’attache généralisées.
DIAGNOSTIQUER UNE PARODONTITE
La parodontite se définit biologiquement comme une maladie inflammatoire chronique multifactorielle associée à un biofilm/plaque dentaire dysbiotique et caractérisée par la destruction progressive du système d’attache des dents. Cliniquement, elle se caractérise par une inflammation gingivale, la présence de poches parodontales, une perte d’attache clinique et une alvéolyse radiographique, conduisant à terme à la perte de dents en raison de mobilités et d’alvéolyses terminales [7].
En clinique, étape par étape, voici comment procéder pour diagnostiquer une parodontite [8].
- Identifier si le patient est atteint de parodontite. Pour ce, le patient devra présenter lors du bilan parodontal (mesure avec une sonde graduée en 6 sites/dent) :
- la présence d’une perte d’attache clinique interdentaire (CAL) détectable sur au moins 2 dents non adjacentes ;
- ou une perte d’attache vestibulaire ≥ 3 mm associée à un sondage > 3 mm détectable sur au moins 2 dents.
Ces pertes d’attache ne doivent pas être attribuables à la présence de récessions gingivales d’origine traumatique, une carie au niveau cervical de la dent, une perte d’attache sur la face distale d’une seconde molaire associée à une malposition ou un site d’avulsion de la dent de sagesse, une lésion endodontique se drainant au travers du parodonte marginal ou encore la présence d’une fracture radiculaire verticale.
- Si une parodontite est diagnostiquée, le bilan parodontal approfondi sera réalisé, incluant le charting (poches parodontales, perte d’attache par mesure du niveau gingival, saignement au sondage…) et l’examen radiographique (panoramique +/- rétro-coronaires +/- rétro-alvéolaires) afin d’identifier le stade et le grade de la parodontite (fig. 3).
Le stade reflète la sévérité de la maladie et sa complexité à être traitée. De I (léger) à IV (complexe), il se définit par une combinaison des marqueurs de sévérité (ex. : perte d’attache, dents perdues pour raisons parodontales) et de complexité de traitement (ex. : profondeur des poches, besoin d’une réhabilitation complexe en raison de versions dentaires ou de la perte de dents pour raisons parodontales) (tab. 2).
Le grade (de A à C) reposera sur des preuves directes de la destruction parodontale sur les 5 dernières années. Celles-ci sont observables par comparaison de l’état actuel avec des clichés radiographiques ou des charting parodontaux antérieurs au RDV. En l’absence de ces éléments, un ratio alvéolyse/âge au niveau de la dent la plus atteinte (à l’exclusion de dents présentant une autre étiologie de l’alvéolyse comme une lésion endoparodontale) sera calculé (tab. 2). De plus, la présence de certains facteurs de risque, tels que le diabète ou le tabagisme, accroît le risque d’évolution de la parodontite et de mauvaise réponse au traitement parodontal. Ainsi, un diabète non équilibré (hémoglobine glyquée HbA1c ≥ 7 %) ou un tabagisme élevé (>10 cigarettes/jour) indiquent un risque élevé (grade C).
- La parodontite sera ensuite diagnostiquée selon son étendue (localisée/généralisée) : si moins de 30 % des dents sont atteintes, elle sera dite localisée. Dans le cas contraire, elle sera dite généralisée. Ceci pourra être complété par la notion de distribution pour indiquer si les secteurs molaires/incisifs sont atteints.
- Enfin, si le patient présente une maladie pouvant influer sur l’état de santé parodontal, cette information pourra être ajoutée comme un descripteur de la maladie. Cela permet de préciser des facteurs systémiques qui influencent la santé parodontale, même s’ils ne sont pas directement liés au stade ou au grade (ex. : lupus…).
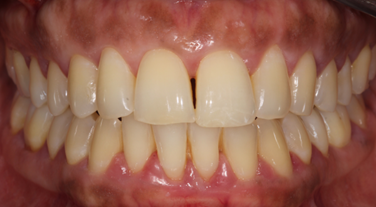
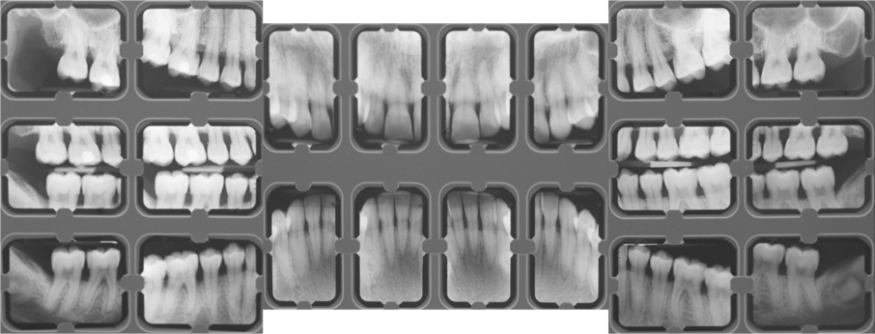
Figure 3. Diagnostiquer une parodontite. Exemple d’une parodontite stade III grade B généralisée.
Mme B., âgée de 38 ans, en bonne santé générale et non fumeuse, présente une parodontite (alvéolyse généralisée comme preuve indirecte de la perte d‘attache et présence de poches lors d’un sondage prospectif). D’un premier abord, la patiente pourrait présenter une parodontite de stade 2, l’alvéolyse n’atteignant que moins de 33 % des hauteurs radiculaires et la patiente n’ayant pas perdu de dents pour raisons parodontales. Or, la patiente présente lors du bilan parodontal des poches atteignant 7 mm et des lésions inter-radiculaires de classe II au niveau de 16 et 27 : elle présente une parodontite de stade 3 (laissant présager de la nécessité d’un traitement parodontal incluant une phase chirurgicale). Concernant le grade, nous ne disposons pas de documents antérieurs de la patiente et nous utilisons le ratio alvéolyse/âge au niveau de la dent la plus atteinte pour poser le grade. Ici, nous avons identifié la 16 et avons un rapport de 30 %/38 ans, soit 0,78 : la patiente présente un grade B. Enfin, plus de 30 % des dents sont atteintes. Le diagnostic est donc parodontite stade 3 grade B généralisée.
Nous invitons le lecteur à consulter un article publié sur le sujet, réalisé à l’occasion de la parution de la nouvelle classification, pour s’approprier plus finement la classification des parodontites [9].
Tableau 2. Classification par stades et grades de la parodontite.
Les parodontites sont classées en quatre stades croissants de gravité. Le stade I marque le début de la perte d’attache, à la frontière entre gingivite et parodontite. Il est réversible avec un traitement précoce axé sur l’hygiène et le contrôle des facteurs de risque. Le stade II correspond à une atteinte modérée avec poches ≤ 5 mm, sans perte dentaire. Le traitement reste non chirurgical, avec un bon pronostic si la maladie est prise en charge. Le stade III se caractérise par des lésions profondes, des pertes d’attache > 5 mm et des pertes dentaires possibles. Une approche chirurgicale peut être nécessaire pour traiter les atteintes complexes. Le stade IV est avancé, avec des destructions sévères, pertes multiples de dents et fonctions masticatoires altérées. Ce stade nécessite une prise en charge globale multidisciplinaire, incluant parodontie, prothèse et parfois orthodontie. Les grades évaluent la vitesse de progression de la parodontite et les facteurs de risque.
Le grade A correspond à une progression lente, sans perte d’attache clinique récente, avec peu de destruction malgré la présence importante de dépôts bactériens et une absence de diabète ou de consommation de tabac. Le grade B indique une progression modérée avec perte osseuse < 2 mm sur 5 ans. Les destructions sont en accord avec la quantité de dépôts, et les patients peuvent être fumeurs légers (< 10 cigarettes/j) ou diabétiques équilibrés. Le grade C reflète une progression rapide, avec perte osseuse ≥ 2 mm en 5 ans. Des destructions sévères sont observées malgré une faible quantité de plaque dentaire. Ce grade est souvent lié à un début précoce, une réponse faible au traitement ou une atteinte localisée (molaires/incisives). Les fumeurs > 10 cigarettes/jour et les diabétiques non équilibrés (HbA1c ≥ 7 %) sont classés en grade C. Cette classification aide à adapter la prise en charge en fonction du risque de progression.
* Au site le plus atteint.
Les recommandations pour le traitement des parodontites de stade I à III
En 2020, la Fédération Européenne de Parodontologie (EFP) a publié les premières recommandations fondées sur des preuves scientifiques pour le traitement des parodontites de stade I à III [3]. Ces recommandations sont issues du Workshop 2019, qui s’est tenu en novembre avec la participation de 90 experts issus de 19 pays. Lors de cet atelier, 15 revues systématiques de la littérature ont été analysées, couvrant l’ensemble des approches thérapeutiques parodontales disponibles. L’objectif de ces travaux était de définir les traitements les plus efficaces, basés sur des données scientifiques solides. Publiées en juillet 2020 dans le Journal of Clinical Periodontology, ces recommandations regroupent 62 propositions thérapeutiques.
Chaque recommandation est classée selon trois niveaux de force, en tenant compte de la qualité des preuves disponibles, du rapport bénéfice/risque, de l’efficacité clinique et du degré d’adhésion des experts (tab. 3). En complément, le niveau de consensus a été évalué pour chaque recommandation, en mesurant le pourcentage d’accord entre les membres du panel (tab. 4).
Ces recommandations ont été reconnues en France par la Société Française de Parodontologie et Implantologie Orale (SFPIO) et le Collège National des Enseignants en Parodontologie (CNEP) : la version française est en accès libre sur les sites web de ces sociétés (voir « Ressources pour aller plus loin »).
Nous allons ici résumer les principales recommandations pour le traitement des parodontites de stade I à III. Nous invitons le lecteur à se référer au document complet de ces recommandations afin d’apprécier l’ensemble des recommandations et les argumentaires complets. Ces recommandations font également référence pour le traitement des parodontites de stade IV. Pour le stade IV, des recommandations spécifiques concernant certains aspects pluridisciplinaires du traitement ont été également proposées lors d’un autre workshop de l’EFP (ex. : contention, traitement orthodontique, réhabilitation prothétique) [4] et ne sont pas abordées ici.
Tableau 3. Force des recommandations : système de notation adopté par l’EFP (source : Association Allemande des Sociétés Médico-Scientifiques et Commission permanente des lignes directrices, 2012).
Tableau 4. Force du consensus : système de notation adopté par l’EFP (source : Association Allemande des Sociétés Médico-Scientifiques et Commission permanente des lignes directrices, 2012).
- Étape 1 : La première étape du traitement vise à instaurer une modification du comportement en motivant le patient à entreprendre une élimination efficace du biofilm dentaire supragingival et à contrôler ses facteurs de risque. Certaines recommandations issues du travail de consensus de l’EFP pour cette phase de traitement sont présentées dans le tableau 5.
Tableau 5. Synthèse de 3 recommandations (sur un total de 10 recommandations) établies pour l’étape 1 du traitement parodontal (d’après Sanz et al, J Clin Periodontol, 2019) – Document traduit en français et disponible sur le site de la SFPIO : https://www.sfpio.com/images/Documents/20210202_EFP_Guideline_FR.pdf
- Étape 2: La deuxième étape du traitement (thérapie étiologique) vise à contrôler (réduire/éliminer) le biofilm et le tartre sous-gingival (instrumentation sous-gingivale). Certaines recommandations issues du travail de consensus de l’EFP pour cette phase de traitement sont présentées dans le tableau 6.
Tableau 6. Synthèse de 6 recommandations (sur un total de 16 recommandations) établies pour l’étape 2 du traitement parodontal (d’après Sanz et al, J Clin Periodontol, 2019) – Document traduit en français et disponible sur le site de la SFPIO : https://www.sfpio.com/images/Documents/20210202_EFP_Guideline_FR.pdf
¥ PPD Pocket Probing Depth = profondeur de sondage de la poche
Si les critères de réussite thérapeutique sont atteints à la réévaluation parodontale (absence de poche parodontale > 4 mm présentant un saignement au sondage), il faut passer à la quatrième étape du traitement. Dans le cas contraire, on passe à l’étape 3.
- Étape 3 : Elle vise à traiter les zones de la denture ne répondant pas de manière adéquate à la deuxième étape de traitement (persistance de poches > 4 mm avec saignement au sondage ou présence de poches parodontales profondes ≥ 6 mm), dans l’objectif de procurer un meilleur accès à l’instrumentation sous-gingivale, ou de régénérer ou réséquer les lésions qui complexifient la prise en charge de la parodontite (lésions intra-osseuses ou atteintes de furcation). Les recommandations issues du travail de consensus de l’EFP pour cette phase de traitement sont présentées dans le tableau 7, et dans les figures 4 et 5 pour les approches chirurgicales des lésions intra-osseuses ou de furcation.
Tableau 7. Synthèse de 1 recommandation (sur un total de 16 recommandations) établie pour l’étape 3 du traitement parodontal (d’après Sanz et al, J Clin Periodontol, 2019) – Document traduit en français et disponible sur le site de la SFPIO : https://www.sfpio.com/images/Documents/20210202_EFP_Guideline_FR.pdf
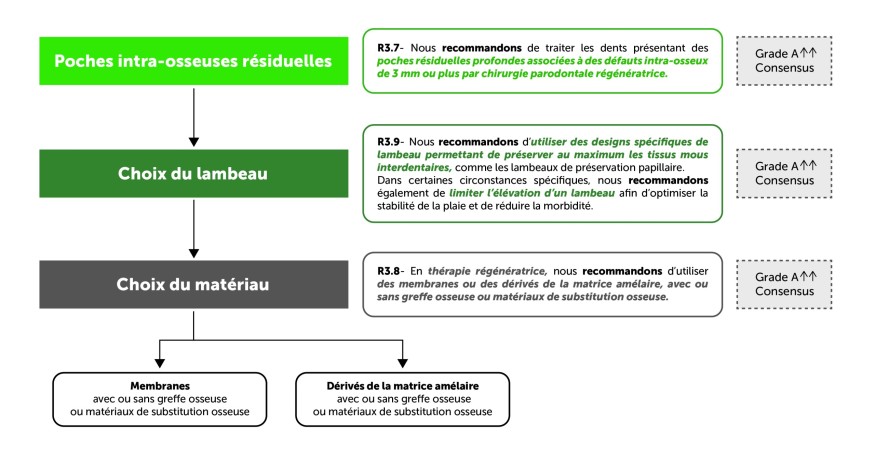
Figure 4. Synthèse de trois recommandations établies pour le traitement régénérateur des défauts intra-osseux associés à des poches résiduelles (au cours de l’étape 3 du traitement parodontal). Pour rappel, une poche intra-osseuse se définit par le fait que le fond de la poche se situe apicalement par rapport à la crête osseuse résiduelle adjacente. La poche est dite profonde quand elle est ≥ 6 mm par rapport au niveau gingival. Dans cette poche intra-osseuse, la lésion intra-osseuse est dite profonde quand elle est ≥ 3 mm par rapport au niveau osseux marginal adjacent. Le traitement régénérateur de ces lésions intra-osseuses profondes, avec des designs de lambeaux préservant au maximum les tissus, se traduit par de meilleurs résultats que la chirurgie avec lambeau d’accès.
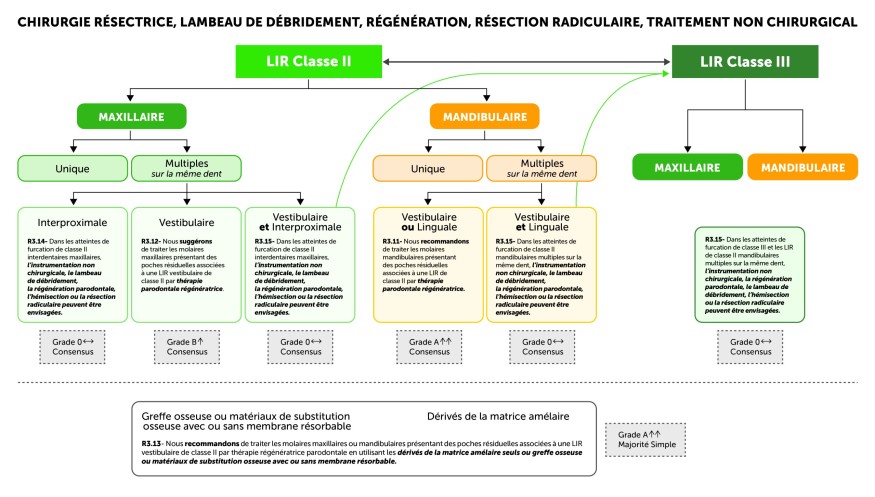
Figure 5. Synthèse de quatre recommandations établies pour le traitement des molaires avec lésions inter-radiculaires de classe II et III associées à des poches résiduelles (au cours de l’étape 3 du traitement parodontal). Notons qu’après traitement chirurgical des molaires avec lésions de furcation de classe II ou III, des taux de survie raisonnables ont été observés sur une période allant de 4 à plus de 30 ans. Globalement, ces taux de survie sont meilleurs pour les atteintes de furcation de classe II que pour celles de classe III. De plus, la conservation de ces dents présente un meilleur rapport coût/efficacité que leur extraction et leur substitution par une prothèse partielle fixe implanto-portée. Enfin, les patients expriment une forte préférence en faveur de la conservation dentaire.
- Étape 4 : La maintenance parodontale vise à maintenir la stabilité parodontale chez tous les patients parodontaux traités, que la parodontite ait été stabilisée ou qu’elle soit en rémission (fig. 1). La maintenance doit être organisée à intervalles réguliers en fonction des besoins du patient. Les recommandations quant à la fréquence de maintenance et son importance sont présentées dans le tableau 8.
Tableau 8. Synthèse de 2 recommandations (sur un total de 20 recommandations) établies pour l’étape 4 du traitement parodontal (d’après Sanz et al, J Clin Periodontol, 2019) – Document traduit en français et disponible sur le site de la SFPIO : https://www.sfpio.com/images/Documents/20210202_EFP_Guideline_FR.pdf
Les recommandations pour l’étape 4 du traitement parodontal présentent des points communs à celles présentées pour les étapes 1 et 2, à savoir :
> l’importance de conseils d’hygiène bucco-dentaire répétés (grade A ↑↑, consensus unanime) avec la possibilité de recourir à une brosse à dents électrique comme alternative à la brosse à dents manuelle (grade O ←→, consensus fort) et de compléter le brossage des dents par un nettoyage interproximal par brossettes interdentaires (grade A ↑↑, consensus unanime) ;
> la possibilité d’utiliser des antiseptiques dans le cadre d’une approche personnalisée (grade O ←→, consensus). Cependant, il n’est pas possible de statuer sur l’utilisation d’autres agents adjuvants (tels les probiotiques, prébiotiques, agents anti-inflammatoires, micronutriments antioxydants) pour le contrôle de l’inflammation gingivale chez les patients en TPS (grade O ←→, consensus sans objet). Parmi les antiseptiques, les dentifrices contenant de la chlorhexidine, du triclosan-copolymère et du fluorure stanneux-hexamétaphosphate de sodium (grade B ↑, consensus) et les bains de bouche contenant de la chlorhexidine, des huiles essentielles et du chlorure de cétylpyridinium (grade B ↑, consensus) sont suggérés ;
> lors de la séance de maintenance, une élimination en routine de la plaque dentaire par PMPR est suggérée (grade B ↑, consensus fort) ;
> le contrôle des facteurs de risque est recommandé chez les patients en thérapeutique parodontale de soutien (grade A ↑↑, consensus fort), principalement le sevrage tabagique et le contrôle du diabète.
Conclusion
Le nouveau système de classification des maladies parodontales, dit de Chicago, appuyé sur la littérature scientifique, est conçu pour être plus simple, clinique et évolutif. Il offre une meilleure lisibilité pour les praticiens tout en restant adaptable aux avancées futures dans la compréhension de la physiopathologie des maladies parodontales. Ce système est enrichi par des recommandations thérapeutiques claires pour les parodontites de stade I à III, fondées sur les données les plus récentes de la littérature scientifique. Il met ainsi en lumière les approches de traitement les plus efficaces actuellement disponibles, dans une optique de maintien à long terme d’une denture saine.
Ressources pour aller plus loin
- Ressources SFPIO sur la nouvelle classification des maladies parodontales: https://www.sfpio.com/informations-praticiens/la-nouvelle-classification-des-maladies-et-affections-parodontales-et-peri-implantaires.html
- Ressources SFPIO sur les recommandations de traitement des parodontites de stade I à III : https://www.sfpio.com/informations-praticiens/traitement-de-la-parodontite-de-stade-i-iii-recommandations-efp-en-pratique-clinique.html
- Si vous désirez télécharger la fiche officielle de la nouvelle classification des maladies parodontales, cliquez ici
Bibliographie
- Caton J G, Armitage G, Berglunch T, Chapple I, Jepsen S. A new classification scheme for periodontal and peri-implant diseases and conditions – Introduction and key changes from the 1999 classification. J Periodontol 2018;89(1):S1-S8.
- Armitage G C. Development of a classification system for periodontal diseases and conditions. Ann Periodontol 1999;4(1):1-6.
- Sanz M, Herrera D, Kebschull M, Chapple I, Jepsen S. Treatment of stage I-III periodontitis-The EFP S3 level clinical practice guideline. J Clin Periodontol 2020;47(22):4-60.
- Herrera D, Sanz M, Kebschull M, Jepsen S, Sculean A. Treatment of stage IV periodontitis: The EFP S3 level clinical practice guideline. J Clin Periodontol 2022;49(24):4-71.
- Chapple I, Mealey B, Van Dyke T, Bartold P, Dommish H. Periodontal health and gingival diseases and conditions on an intact and a reduced periodontium: Consensus report of workgroup 1 of the 2017 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions. J Periodontol 2018;89(1):S74-S84.
- Tonetti M, Greenwell H, Kornman K. Staging and grading of periodontitis: Framework and proposal of a new classification and case definition. J Periodontol 2018;89(1):S159-S172.
- Papapanou P, Sanz M, Buduneli N, Dietrich T, Feres M. Periodontitis: consensus report of workgroup 2 of the 2017 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions. J Periodontol 2018;89(1):S173-S182.
- Tonetti M S, Sanz M. Periodontitis: clinical decision tree for staging and grading. [en ligne]. Téléchargeable à cette adresse : https://www.efp.org/fileadmin/uploads/efp/Documents/Campaigns/New_Classification/Guidance_Notes/report-02b.pdf
- Nisand D, Gosset M, Vincent-Bugnas S. Une nouvelle classification des maladies parodontales. L’information dentaire 2019, p. 16-26.









Commentaires